《Science》重磅: 从毛细血管到整个心脏!3D打印助力重建心脏
《Science》重磅: 从毛细血管到整个心脏!3D打印助力重建心脏普逻迈 3D部落 昨天一、研究背景
生、老、病、死是人类不可避免的问题,我们从生下来以后,就逐渐走向死亡,会慢慢衰老,会生病。生物技术在治疗人类疾病及衰老方面起着至关重要的作用。生物制造的目标是设计组织支架来治疗选择有限的疾病,如晚期器官衰竭。3D生物打印已经在微生理器件,模式化组织,可灌注的血管网络和可植入支架等方面取得了重要的里程碑。然而,直接打印活细胞和软物质生物材料,如细胞外基质蛋白已经被证明是困难的。一个关键性的障碍是如何在打印过程中支持这些柔软和动态的生物材料,以达到重建复杂3D结构和功能所需的分辨率和保真度。最近,Dvir和他的同事将一种脱细胞的细胞外基质水凝胶打印到一个类似心脏的模型中,结果表明,人类心肌细胞和内皮细胞可以整合到打印中,并在培养1天后以球形中立细胞的形式出现。然而,他们没有进行进一步的结构或功能分析。
胶原蛋白在细胞外基质中发挥着至关重要的作用,因此它是一种理想的生物制造材料。在细胞外基质中,胶原蛋白提供了机械强度,使细胞和组织间的结构组织得以分开,并作为细胞粘附和信号分子的仓库。然而,由于胶原蛋白的凝胶化通常是通过热驱动的自组装来实现的,很难控制,因此很难用天然未改性的胶原蛋白来构建3D生物打印的复合支架。研究人员已经使用了一些方法来改性胶原蛋白制备水凝胶,包括用化学方法将胶原蛋白改性成紫外可交联的,以及通过调整pH值、温度和胶原蛋白浓度来控制凝胶化和打印保真度,或将其变性成凝胶以使其具有热致可逆性。然而,这些水凝胶通常是柔软的,容易下垂,因此它们很难打印出超过几层高度的高保真度。

二、研究成果
胶原蛋白是人体细胞外基质的主要成分。使用胶原蛋白支架来制备具有复制组织、器官的结构和功能已被证明是一个挑战性的问题。美国卡内基梅隆大学Feinberg教授团队提出了一种利用自由的可逆嵌入悬浮水凝胶(FRESH)来对胶原蛋白进行3D生物打印,这种方法能够在不同的尺度上直接获得具有精确控制组成和微观结构的人心脏组织成分,从毛细血管到整个器官。通过控制pH驱动的凝胶不仅可以提供20微米的细丝分辨率,而且还可以获得能够快速细胞渗透和微血管化的多孔结构,以及提供用于制造和灌注多尺度血管系统和三叶瓣膜的机械强度。作者发现通过微型电脑断层扫描技术可以证明3D生物打印的FRESH心脏可以精确地复制患者特有的解剖结构。此外,用人类心肌细胞打印的心室显示同步收缩,定向动作电位传播,以及在收缩高峰期壁增厚高达14%。该工作发表在《Science》上。

三、图文速递
图1. 使用FRESH v2.0水凝胶对胶原蛋白进行高分辨率的3D生物打印。
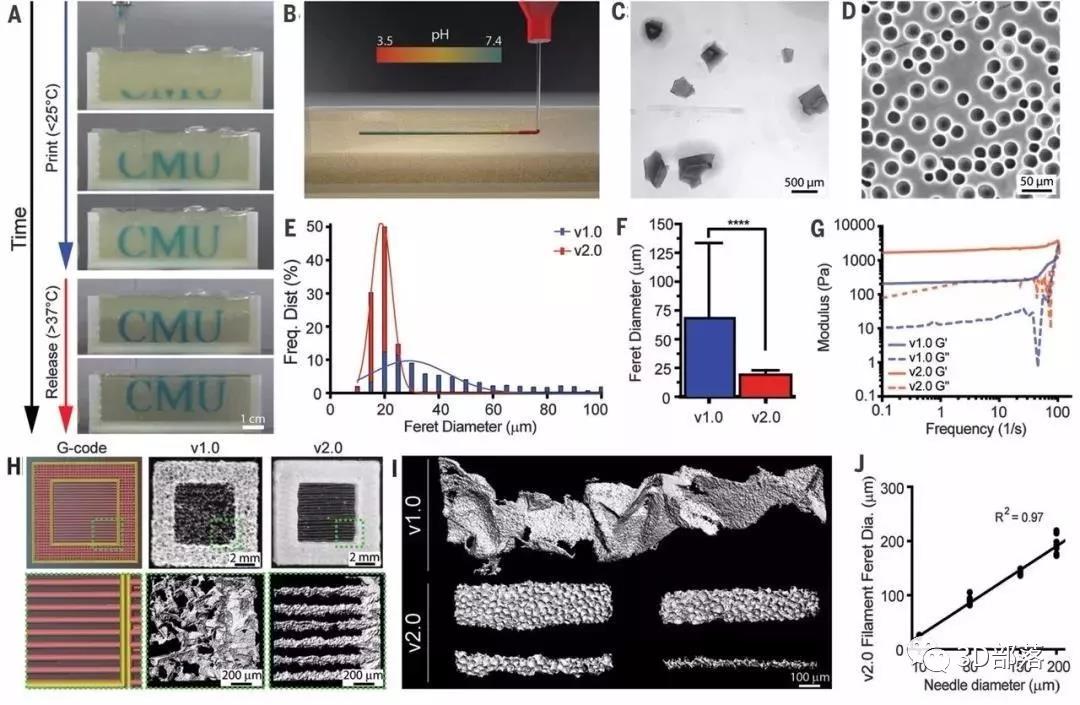
(A) 3D打印字母的延时序列。(B) 将酸化的胶原蛋白溶液挤出到pH 7.4的FRESH支撑液中,快速中和使胶原蛋白凝胶化,形成胶原蛋白丝。(C) FRESH v1.0和(D) FRESH v2.0支撑液中明胶微粒的代表性图像,显示尺寸和多分散性下降。(E) FRESH v1.0 (蓝色)和FRESH v2.0 (红色)中明胶微粒的直径分布直方图。(F) FRESH v1.0和FRESH v2.0中明胶微粒平均直径[N > 1200]。(G) 在FRESH v1.0和FRESH v2.0支撑液中,存储模量(G)和损耗模量(G)显示屈服应力流体行为。(H) 中间具有单纤维的“窗口框架”的打印结构,分别来自于G-编码(左)、FRESH v1.0(中)和FRESH v2.0(右)。(I)使用FRESH v1.0打印单丝胶原蛋白(顶部),以及 FRESH v2.0打印直径为20 - 200mm的相对光滑的丝状胶原蛋白(底部)。(J) FRESH v2.0获得的胶原纤维直径作为挤出针内径为的函数,呈线性关系。
图2. FRESH的3D生物打印构建可灌注的胶原血管和微孔胶原蛋白支架,可促进体内微血管的形成。
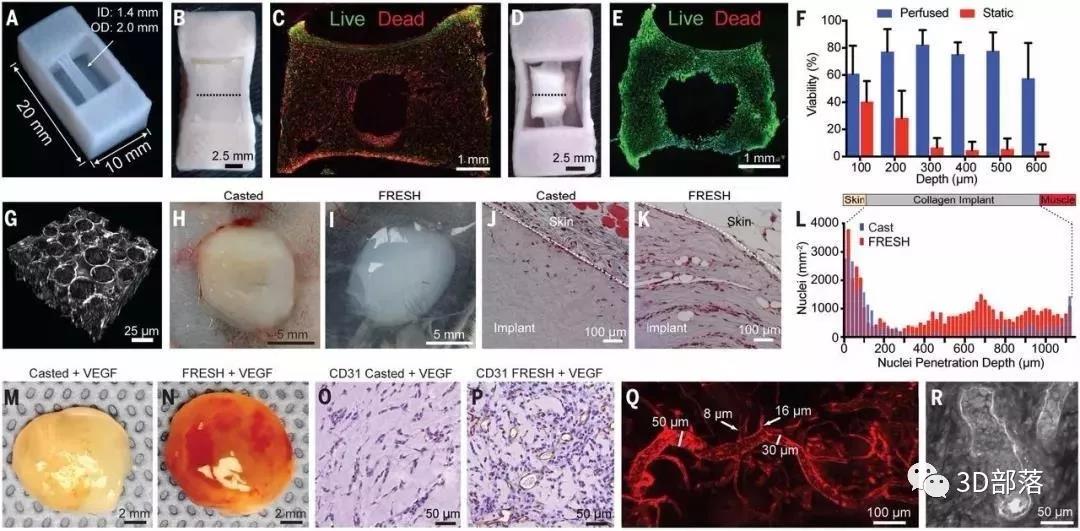
(A) FRESH打印的胶原蛋白管结构。(B) 将C2C12细胞与胶原凝胶混合物在胶原蛋白管周围铸型,静置培养5天。(C) 来自于(B)的活细胞(绿色)和死细胞(红色)的组织横切面。(D)将C2C12细胞与胶原凝胶混合物在胶原蛋白管周围铸型,灌注5天。(E) 来自于(D)的活细胞(绿色)和死细胞(红色)的组织横切面。(F) 细胞存活率作为组织表层深度的函数。(G)从支撑液中移除明胶微粒后,多光子成像显示FRESH打印的胶原结构中的微尺度孔隙。(H和I) 皮下植入7天后,胶原蛋白构建无VEGF的模型(H)和FRESH打印(I)。(J和K) 马森三色染色观察细胞(红色)和胶原蛋白(蓝色)。(L) 植入后细胞密度作为铸型和FRESH打印的胶原盘深度的函数。(M和N) 皮下植入10天后,用VEGF (100 ng/ml)处理构建胶原模型(M)和FRESH打印(N)。(O和P) 皮下植入10天后,注入VEGF (100ng /ml)的铸型(O)和FRESH打印(P)的胶原盘CD31染色(棕色)和细胞(蓝色)。(Q)凝集素尾静脉注射标记的FRESH打印胶原盘内宿主血管浸润(直径8 ~ 50mm)(红色)。(R)进入FRESH打印的结构70毫米的多光子图像,显示微血管系统腔内的红细胞。
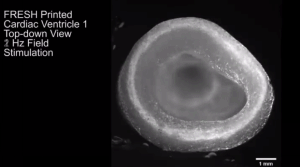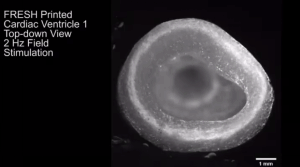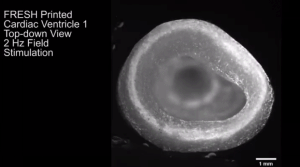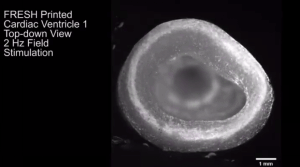
图3. 可收缩的FRESH 3D生物打印的人心室模型。
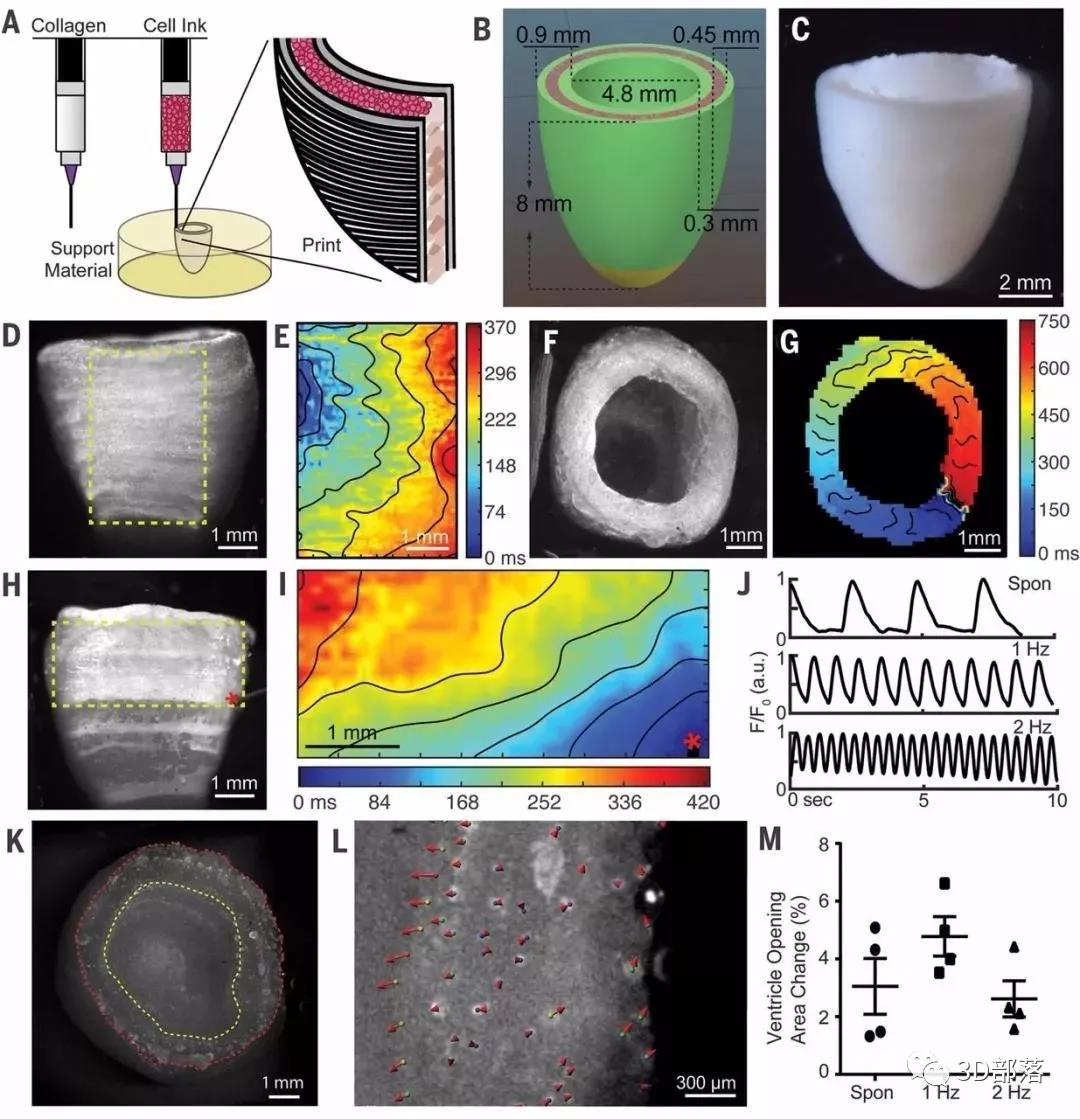
(A) 使用胶原蛋白墨水和高浓度细胞墨水进行双材料FRESH打印的示意图。(B) 心室模型,心肌细胞的中心部分 (粉红色),内外胶原蛋白壳(绿色),仅含胶原蛋白的切片(黄色)。(C) FRESH打印的心室显微图。(D) 钙敏感染料染色的FRESH打印的心室侧视图,显示细胞分布均匀。(E) 子区域的钙图谱[(D)中的黄色框],显示自发的、定向的钙波传播,传导速度为1.97 cm/s。(F) 用钙敏感染料染色的FRESH打印的心室俯视图。(G) 钙谱显示自发圆钙波在心室周围传播,传导速度为1.31 cm/s。(H) 用钙敏染料染色的FRESH打印的心室穴位刺激(红色星号表示电极位置)。(I) 子区域[(H)中的黄色框]的钙映射,显示了纵向传导速度为2.0 cm/s的各向异性钙波传播。(J) 自发收缩时的钙瞬态轨迹(上)、1-Hz场刺激(中)和2-Hz场刺激(下)。钙荧光强度(F)通过除以基线荧光强度(F0)归一化。(K) FRESH打印的心室自上而下的图像,内室(黄色)和外室(红色)的轮廓。(L) 分析1-Hz场刺激时心室壁的一个分区的位移,显示室内外壁的运动;大小和方向用红色箭头表示。(M) 在收缩期峰值时心室内室横截面积(N = 4)。
图4. 器官规模的FRESH 3D生物打印的三叶心脏瓣膜和多尺度血管系统,以及新生儿规模的心脏。
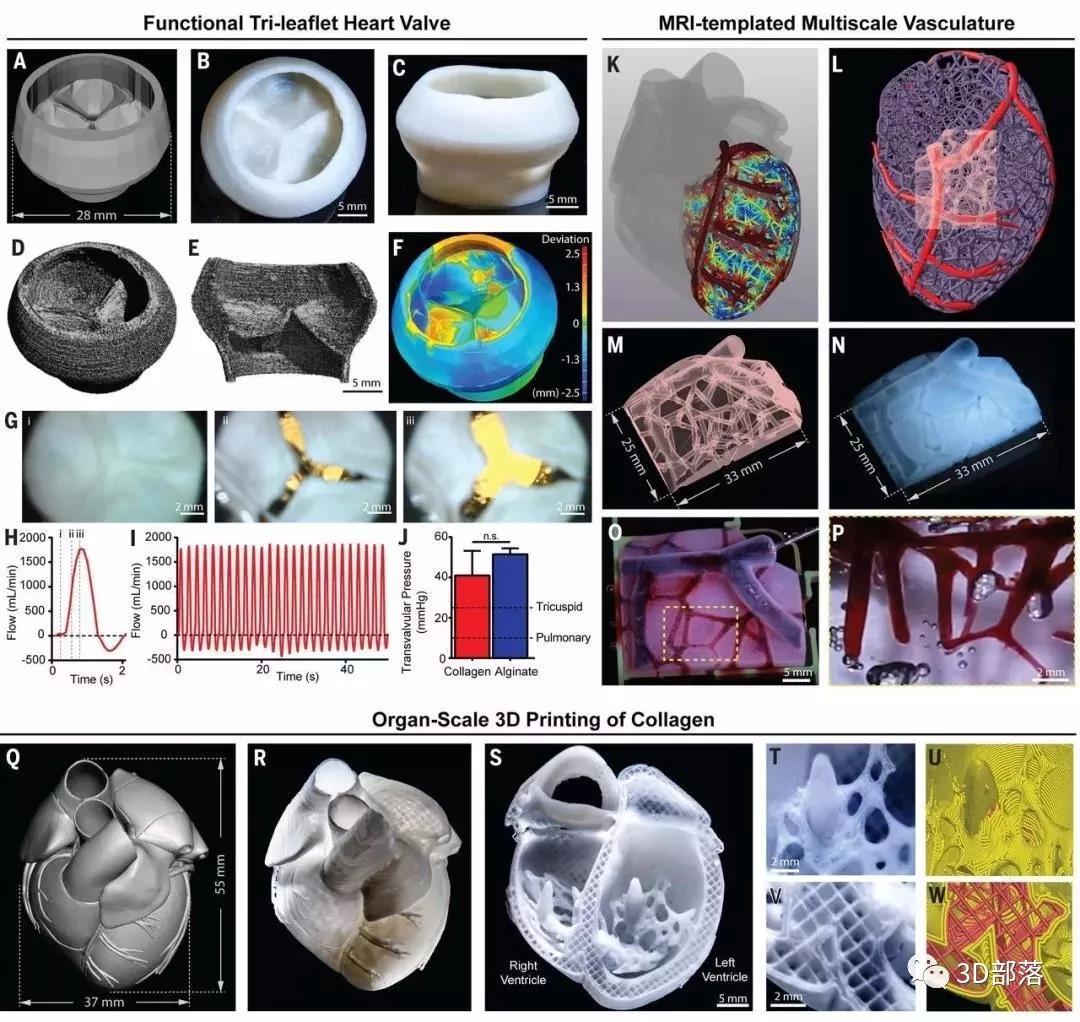
(A) 成人规模的三叶心脏瓣膜的三维模型。(B和C) FRESH 3D打印的胶原心瓣膜顶部和侧面图,添加硫酸钡作x线对比。(D) uCT重建显示全打印阀门。(E) 侧壁和单张的横截面。(F) 对uCT三维表面与三维模型进行定量测量,平均上印量为+0.55 mm,下印量为-0.80 mm。(G) 脉动流量超过1秒时阀门开启顺序。(H) 一个单循环内的多普勒血流速度测量: (i)关闭、(ii)半开和(iii)打开。(I) 与(H)在多个周期内相同。(J) 与天然阀门工作压力相比,打印好的藻酸盐和胶原蛋白阀门的最大跨瓣压力[N = 3]。(K) 通过计算得到的具有左心室多尺度血管网络的MRI衍生的 3D人类的心脏模型(灰色)。左冠状动脉前降支(红色)是引导小尺度血管形成的模板,小尺度血管的直径随着离冠状动脉(红色到蓝色)的距离而减小。(L) 左心室的冠状动脉前降支(红色),计算生成的脉管系统(紫色)和感兴趣的子区域(粉红色)。(M) 透明区显示血管网络三维结构。(N) FRESH生物打印的胶原蛋白子区域,显示血管网络的再生。(O) 相互连接的经过冠状动脉使用甘油灌注血管网络(红色)。(P) 胶原蛋白经光学清除并灌注甘油(红色),显示灌注至直径约100 mm的血管。(Q) 按新生儿大小缩放的MRI衍生的3D人类心脏。(R) FRESH打印的胶原蛋白心脏。(S) 胶原蛋白心脏横切面,显示左右心室和内部结构。(T和U) 左心室骨小梁的高保真图像(T),显示从G-编码复制的复杂的解剖结构(U)。(V和W)心室之间隔膜的高保真图像(V),显示了从G-编码复制的方格子填充(W)。
四、研究小结
这种3D生物打印技术使用快速的pH值变化来驱动胶原蛋白在缓冲支撑材料中进行自组装,使得能够:
(1)使用未经化学修饰的胶原蛋白作为生物墨水,
(2)使用12至24 mg/ml的高胶原蛋白浓度来增强机械性能,
(3)创建复杂的组织结构和功能。虽然只用了人类的心脏来证明这个概念,但是FRESH的3D生物打印技术是打印胶原蛋白是一个平台,可以发展成适用于多种器官体系的先进组织支架。
在这个过程中,仍有许多挑战需要克服,如产生组织所需的数十亿细胞需要对大型组织进行3D生物打印,实现规模生产,以及为临床应用建立一个监管机制。虽然一个功能齐全的器官的3D生物打印尚未实现,但我们现在有能力去开始构建原生组织的结构、机械和生物学特性。
五、参考文献信息及链接
A. Lee*, A. R.Hudson*, D. J. Shiwarski1, J. W. Tashman, T. J. Hinton, S. Yerneni, J. M.Bliley, P. G. Campbell, A. W. Feinberg, 3D bioprinting of collagen to rebuild componentsof the human heart, Science, 2019, 365, 482–487. DIO: 10.1126/science.aav9051.https://science.sciencemag.org/content/365/6452/482
(来源:高分子科学前沿 作者:刘雄)

医用PEEK 3D打印机 3dpro 牛魔王3
- 上一篇:色彩的真谛!是什么让3D打印
- 下一篇:根治秃顶的时代即将到来?干细